候选药物的水溶性差对制剂科学家实现有效口服给药提出了巨大挑战。溶解性差通常与溶解行为差有关,进而当肠道吸收受到溶解速率限制造成这类药物的生物利用度差。布洛芬(IBU)在胃肠水溶液中的溶解性差、溶出率低,限制了其应用、吸收、分布、靶器官递送和生物利用度。近年来,全国多个研究团队尝试开发了电纺聚合物纳米纤维,以解决生物制药分类系统(BCS)II类药物布洛芬的水溶性差的问题。亲水性可纺聚合物,如环糊精,醋酸纤维素,乙烯吡咯烷酮和聚己内酯等被用作制造纳米纤维的载体系统。科学家们努力尝试优化静电纺丝参数,如流速、电压和喷丝头到收集器的距离。利用扫描电子显微镜和差示扫描量热法对制备的布洛芬负载纳米纤维进行表征分析。还进行了药物释放研究和离体肠道吸收研究。与纯布洛芬晶体相比,基于纳米纤维的平台显著改善了布洛芬的体外吸收。
快速溶解的口腔膜是常以亲水聚合物如明胶、淀粉、羧甲基纤维素制备(CMC) 羟丙基纤维素 (HPC) 果胶,海藻酸盐,壳聚糖,普鲁兰多糖,聚乙烯吡咯烷酮(PVP)、聚乙二醇(PEO)、聚乙烯醇(PVA)。生产快速溶解的口腔膜的常用技术是薄膜浇铸或热熔法将活性化合物分散并封装于亲水层中的挤出法快速溶解的口服膜应具有一定的力学完整性。
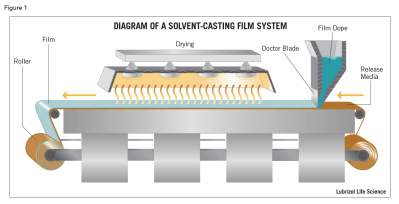
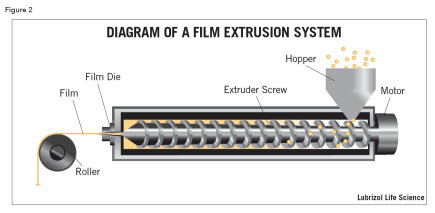
两种方法在薄膜制造中占主导地位:溶剂浇铸(Figure 1)和热熔挤出(Figure 2)。两者各有利弊,具体取决于所用 API 的性质和最终产品所需的特性。1
来源(网络)
来源(网络)
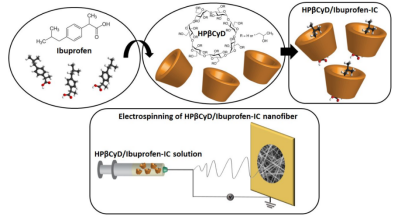
下图是布洛芬和羟丙基-β-环糊精的化学结构。布洛芬与羟丙基-β-环糊精分子之间包合物形成的示意图,以及羟丙基-β-环糊精/布洛芬包合物纳米纤维的静电纺丝的技术原理。2
来源(网络)
下图(Figure 14)是罗切斯特大学哈吉姆工程与应用科学学院Melodie Lawton团队使用聚己内酯(PCL)和聚乙烯吡咯烷酮(PVP)的混合物制成的口腔粘膜布洛芬(IBU)递送的功能性电纺纳米纤维贴片,他们研究发现用于药物递送和纤维形成的最佳共混物是PCL:PVP的比例为70:30。3

来源(网络)
下视频是康奈尔大学Asli Celebioglu团队用纯布洛芬粉末、羟丙基-β-环糊精/布洛芬(1∶1)和羟丙基-β-环糊精/布洛芬(2∶1)包合物纳米纤维的静电纺丝在蒸馏水中的溶解效果。
REFERENCE:
1.https://lubrizolcdmo.com/technical-briefs/dissolving-films/
2.DOI: 10.1021/acs.molpharmaceut.9b00798
3.https://www.hajim.rochester.edu/senior-design-day/development-of-pcl-pvp-nanofibers-patches-for-pediatric-ibuprofen-oral-mucosa-delivery/
【版权声明】本文部分图片、文字、字体来源于互联网,版权归原作者所有,仅供学习参考之用,禁止用于商业用途,如有侵权,请联系删除